Poreklo kompleksnosti u životu je, samo po sebi, komplikovana tema. Ali osnove se mogu relativno jednostavno i lako objasniti u kratkom tekstu, i za njih nije potrebno posebno predznanje nauke. Ovaj tekst sadrži objašnjenje, na najosnovnijem nivou, nekoliko osnovnih pojmova iz hemije i biologije; zatim, na osnovu tih pojmova, objašnjava šta znamo o nastanku kompleksnosti u univerzumu u kome živimo.
Počnimo od objašnjenja…
1. Elektronegativnost, voda, i priroda hidrofobičnosti
Kao što danas praktično svi ljudi već znaju, atomi se sastoje od jezgra (koje se sastoji od protona i neutrona) okruženog elektronima. Ali većina ljudi zamišlja ove elektrone kao čestice – male kuglice koje se okreću oko jezgra isto kao Mesec oko Zemlje. Ovo nije tačna slika: elektroni se u atomima i molekulima pojavljuju u vidu kompleksnih oblasti naelektrisanja, koje se mogu opisati kroz jednačine kvantne fizike.
Ali pošto nećemo ovde ulaziti u kvantnu mehaniku, upotrebićemo jednu analogiju koja prilično dobro opisuje pravo stanje stvari. Umesto čestice, možemo o elektronu razmišljati kao o oblaku naelektrisanja koji okružuje atom. Možemo to da prikažemo na sledeći način:

Molekuli nastaju kada se atomi povežu kovalentnim vezama. Ove veze nisu ništa drugo do par elektrona koji istovremeno pripada i jednom i drugom atomu. U okviru naše sheme, ovo možemo da zamislimo kao stapanje “elektronskih oblaka.” Molekul fluora, F2, bi izgledao kao na sledećoj slici:
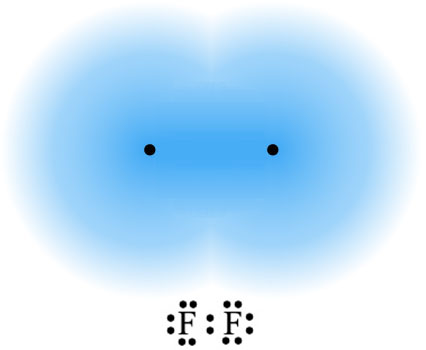
Ovde u igru ulazi jedan dodatni pojam: elektronegativnost, koju možemo za naše potrebe definisati kao “snagu kojom atomi privlače elektrone.” Veoma elektronegativan element, kao što je fluor, teži da privuče ka sebi ne samo svoje sopstvene elektrone, već i elektrone iz kovalentne veze sa drugim atomima. Na gornjoj slici je molekul u kome dva atoma fluora jednakom snagom vuku elektrone prema sebi, zbog čega su oni ravnomerno raspoređeni.
Ali šta se događa u vezama u kojima dva atoma imaju nejednaku elektronegativnost? U tom slučaju, elektronegativniji element teži da ka sebi privuče elektrone iz veze. Recimo, ako povežemo slabo-elektronegativni vodonik sa snažno-elektronegativnim fluorom, dobijamo sledeću situaciju:
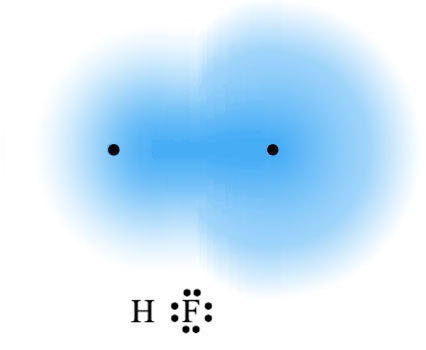
Ovo ima jednu veoma važnu posledicu. Broj protona u molekulu F2 je jednak broju elektrona, pozitivna i negativna naelektrisanja se međusobno potiru, i otud, molekul je što se elektromagnetizma tiče neutralan. U molekulu HF, broj protona je takođe jednak broju elektrona, naelektrisanja se potiru…i molekul bi trebalo da bude neutralan.
Ali zbog neravnomernog rasporeda elektrona, to više nije slučaj. Kraj molekula na kome se nalazi fluor će biti više negativno naelektrisan, pošto elektroni teže da provedu više vremena na tom kraju. Istovremeno, “oblak” oko jezgra atoma vodonika se istanjio, zbog čega mali deo pozitivnog naelektrisanja može da “procuri” napolje. Otud, ovaj molekul se ponaša kao mali naelektrisani “štapić”, sa jednim pozitivnim i jednim negativnim krajem.
Da bi smo se od ovih hemijskih stvari malo približili životu i biologiji, razmotrimo kakav uticaj ovo ima na molekul vode.
Svi znaju formulu vode: H2O, dva atoma vodonika i jedan atom kiseonika. Ali elektronegativnost kiseonika je značajno veća nego elektronegativnost vodonika. Ako zamislimo elektronski oblak oko molekula vode, i označimo pozitivno naelektrisanje plavom bojom, neutralno zelenom, a negativno crvenom, taj molekul bi izgledao kao na sledećoj slici (levo):
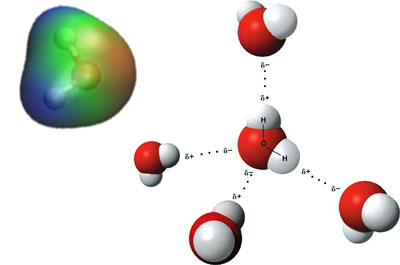
Molekuli vode su jako retko usamljeni: naše telo se uglavnom sastoji od vode, u kojoj je sve ostalo rastvoreno. Šta se događa u tečnoj vodi, u kojoj se ogroman broj ovakvih molekula nalazi u neposrednoj blizini (jedan litar vode se sastoji od otprilike 33,000,000,000,000,000,000,000,000 molekula)?
Pozitivno naelektrisanje privlači negativno. Svaki pozitivan “krak” molekula vode će privući negativni kiseonik nekog susednog molekula. Svaki negativan kiseonik će privući dva pozitivna kraka susednih molekula. Ova privlačna sila se naziva vodonična veza.
Zbog ovoga, voda se ponaša kao velika trodimenzionalna mreža, koja se neprestano reorganizuje. Slučajni pokreti molekula izazivaju stalno pucanje vodoničnih veza, i stvaranje novih, hiljadama milijardi puta u sekundi. Ovo je razlog zbog koga čovek koji skoči “na stomak” u bazen doživi bolno iznenađenje: voda je veoma nekompresibilna, i u naglom udarcu tela o površinu, ponaša se skoro kao čvrsta površina. S druge strane, ako zaronimo ruku u vodu, nemamo problema sa time, jer se mreža vodoničnih veza reorganizuje oko naše ruke u toku njenog ulaženja.
Ovo nas dovodi do poslednjeg koncepta koga treba razumeti u ovom odeljku: hidrofobičnost. Ovaj termin znači “boji se vode”, i važi za supstance kao što je ulje, koje se ne mešaju sa vodom. Ali zašto se ne mešaju?
Molekuli ulja su prevashodno sastavljeni od atoma ugljenika i vodonika, koji su približno iste elektronegativnosti. Otud, ovi molekuli su elektirčno neutralni – elektroni su raspoređeni ravnomerno, i nema tačaka pozitivnog ili negativnog naelektrisanja. Otud, kada ulje uđe u vodu, voda ne može da pravi vodonične veze sa molekulima ulja.
Ovo samo po sebi nije nikakav problem, ali postavlja jednu energetsku zamku. Uzmimo da smo ubacili u vodu tri molekula ulja, koji sada slobodno plutaju kroz vodu. Svaki molekul ulja je okružen molekulima vode. Ti molekuli vode su ograničeni: ona strana molekula vode koja je okrenuta ka molekulu ulja ne može da učestvuje u vodoničnim vezama. Pogledajmo ovo shematski na slici (levo):
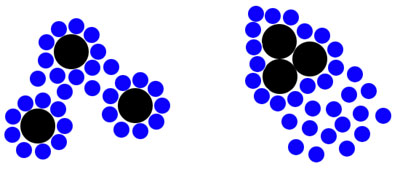
Na slici, molekuli vode (plave tačke) okružuju molekule ulja (veće crne tačke).
Svi molekuli u ovom rastvoru su u stalnom pokretu, i molekuli ulja će biti bacani kroz vodu na sve strane. Dok se jednom ne desi da dva ili više molekula ulja nalete jedan na drugog. I tu leži odgovor na pitanje hidrofobičnosti.
Više molekula vode je potrebno da se okruže pojedinačni molekuli ulja, nego što treba da se okruži skupina takvih molekula. Pogledajte gornju sliku, sa desne strane: na obe strane se nalazi isti broj molekula vode, ali kao što možete videti, na desnoj slici je veliki broj tih molekula sada slobodan – više nije u kontaktu sa uljem
Kada se jedan molekul ulja kreće kroz vodu, to je energetski neutralna akcija: ako se ispred ulja pokida veza između dva molekula vode, iza će se napraviti nova. Ali kada se molekuli ulja skupe na gomilu, sada oslobođeni molekuli vode odjednom formiraju sve vodonične veze koje mogu. Ako sad molekul ulja želi da napusti ovu skupinu, on mora da uloži energiju u kidanje postojećih vodoničnih veza koje neće biti nadoknađene – pošto bi molekuli vode opet postali ograničeni u broju veza koje mogu da naprave.
Zbog ovoga, molekuli ulja bivaju “gurnuti” na gomilu od strane molekula vode. Kao što svako može da vidi u pilećoj supi: kapi ulja se brzo skupe i isplivaju na površinu vode. (Ako koristimo ulje koje je teže od vode, isto bi se desilo, samo bi kapi bile izolovane na dnu posude.)
Sada smo definisali osnovne pojmove koji su potrebni za razumevanje dalje priče. Ali nismo još gotovi sa učenjem! Potrebno je da se još pozabavimo nekim osnovnim idejama u vezi strukture i funkcije proteina.
2. Proteini, njihovo savijanje, i njihova struktura
Proteini su fantastično fleksibilni molekuli. Oni mogu biti strukturalni: koža i vezivna tkiva se dobrim delom sastoje od dugih lanaca proteina zvanog kolagen. Mogu vršiti mehanički rad: sila koja pokreće naše mišiće nije ništa drugo do serije hemijskih reakcija u kojima se protein miozin pomera niz lanac sastavljen od proteina zvanog aktin. Praktično svi biohemijski procesi u telu zavise od proteina (koji se u ovom slučaju zovu enzimi): da bi se pojedeni šećer pretvorio u energiju, na primer, potrebna je serija reakcija koju vrši ukupno jedanaest različitih proteina.
Ali kako dolazi do ove fleksibilnosti?
Deo odgovora na ovo pitanje se nalazi u hemijskom sastavu proteina. Proteini su lanci sastavljeni od jedinica zvanih amino-kiseline. Postoji dvadeset standardnih amino-kiselina, koje koriste praktično svi živi organizmi na zemlji (mnogi dodaju i neke nestandardne na ovaj broj), i one su hemijski veoma raznovrsne.
Dobar deo amino-kiselina ima grupe koje mogu da učestvuju u hemijskim reakcijama: baze, kiseline, alkoholi… Ali najveći deo se sastoji od hidrofobičnih grupa različitih veličina i oblika, koje retko imaju bilo kakvu direktnu funkciju u biohemiji.
Na osnovu informacija pohranjenih u genima, amino-kiseline se kombinuju u lanac; svaki protein sadrži amino-kiseline poređane po određenom redosledu, i ovaj redosled čini svu razliku između različitih proteina. Ali kako jedan prost lanac hemijskih jedinjenja može da vrši sve funkcije potrebne za život?
Odgovor je da ne može. Lanac amino-kiselina je samo osnovna, primarna struktura proteina. Protein ne može da funkcioniše dok se pravilno ne savije. A u ovom slučaju, reč “savijanje” ima veoma, veoma specifično značenje…
Zamislimo proteinski lanac u svetu svega onoga o čemu smo pričali u ovom tekstu. Neke karike u lancu su pozitivno ili negativno naelektrisane: one će privlačiti jedne druge. Neke su sastavljene od atoma nejednake elektronegativnosti, i one će početi da formiraju vodonične veze jedne sa drugima, a i sa okolnom vodom. Konačno, najvažnije od svega, veliki deo karika je hidrofobičan: isto kao sa uljem, voda će ove karike da gurne na gomilu.
Ovo dovodi do komplikovanog kolapsa lanca, koji zavisi od reda i prirode amino-kiselina koje ga čine. Nakon kolapsa, ovaj lanac postaje nešto daleko komplikovanije: protein, čija trodimenzionalna struktura definiše njegovu funkciju.
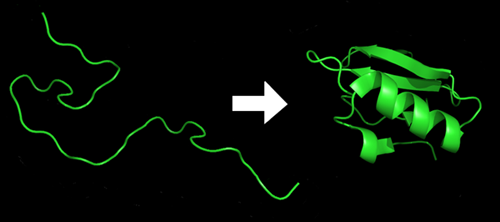
Pravilno savijanje proteina je apsolutno neophodno za njegovu funkciju. Postoji gomila genetskih bolesti kod kojih se protein i dalje normalno proizvodi u telu, ali zbog greške u lancu ne uspeva da se pravilno savije u potrebnu strukturu. Dobar primer su genetski defekti slabih kostiju: zbog greške u strukturi kolagena, on se ne savija kao što je potebno, i nema potrebnu snagu da održi kost na okupu. Takođe, mnoge bolesti nastaju zbog spore akumulacije nepravilno savijenih proteina: Alchajmerova bolest je rezultat nepravilnog savijanja dva proteina u okviru nervnih ćelija.
Ovaj proces može čak i da bude zarazan. Protein koji se pogrešno savije može da postane katalizator koji navodi druge proteine iste vrste da se pogrešno saviju, izazivajući lančanu reakciju koja na kraju vodi do teških posledica. Bolest “ludih krava” je ovde standardan primer: nepravilno savijen protein iz bolesnih krava prodire u mozak, i tamo izaziva nepravilno savijanje proteina neophodnih za normalnu funkciju nervnog sistema.
U slučaju enzima, njihova funkcija je u potpunosti zasnovana na ovoj trodimenzionalnoj strukturi. Enzimi poseduju takozvanu “aktivnu oblast”: deo trodimenzionalne strukture čiji oblik odgovara nekoj specifičnoj hemikaliji. Recimo, enzim heksokinaza, prvi u lancu potrebnom za pretvaranje šećera glukoze u energiju, ima “džep” koji po obliku i naelektrisanju posebno udobno prima baš molekul glukoze. Onda, povrh toga, hemijske grupe kritičnih amino-kiselina u enzimu su raspoređene tako da maksimalno pomažu odvijanju potrebne reakcije. Bez ovih osobina, funkcionisanje enzima bi bilo potpuno nemoguće.
A ovo savijanje se odvija “na slepo”, na osnovu prostih pravila i zakona elektromagnetizma: pozitivno privlači negativno, atomi imaju različite elektronegativnosti, voda automatski gura hidrofobične supstance na gomilu. I na osnovu ove “jednostavne” interakcije, lanac sastavljen od povezanih “kuglica” različitog naelektrisanja se pretvara odjednom u molekularnu mašinu, sa pokretnim delovima, pravilno pozicioniranim hemijskim grupama, itd.
3. Funkcija proteina
Vredi razmotriti, za kraj, još jednu veoma bitnu stvar: kako se funkcija proteina zaista izvodi u okviru ćelije. Uzmimo ovde kao primer replikaciju DNK.
Da bi se majka-ćelija podelila na dve nove ćerke-ćelije, ona mora da iskopira svoju DNK. Onda u deobi, jedna kopija ostaje u jednoj, a druga u drugoj ćerci-ćeliji. Proces replikacije je kompleksan, i uključuje aktivnost više različitih proteina; ali radi jednostavnosti, ignorisaćemo većinu komplikacija i koncentrisaćemo se na samo jedan proces.
Kao što smo svi videli na televiziji, u filmovima, a kao što se i uči u školi, DNK se sastoji od dva lanca koja su povezana jedan sa drugim. Ovi lanci se sastoje od četiri različite baze – adenina, guanina, timina i citozina, koji se obično označavaju slovima A, G, T i C, respektivno. Ako se na jednom lancu DNK nalazi adenin (A), on može da sa timinom (T) na suprotnom lancu da uspostavi dve vodonične veze. Takođe, guanin (G) može da uspostavi tri vodonične veze sa citozinom (C). Dva lanca DNK se sastoje od ovako povezanih baznih parova, proizvodeći nešto što liči na merdevine povezane u sredini nizom vodoničnih veza: lanci su strana merdevina, a svaki AT ili GC bazni par je po jedna stepenica. Zbog raznih razloga, ove “merdevine” su zatim “zavrnute” u spiralu, tako da dobijamo nešto slično ovome:
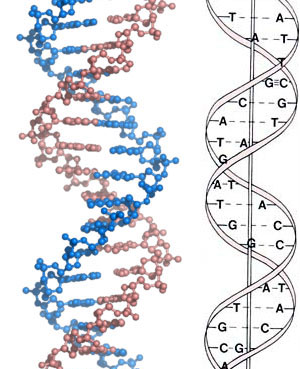
Da bi se DNK iskopirala, ova dva lanca se razdvoje, i svaki se kopira posebno. Iz raznih razloga u koje nećemo ovde ulaziti, jedan lanac (3′->5′) se kopira na prilično komplikovan način, dok se drugi lanac (5′->3′) kopira jednostavno. Koncentrisaćemo se na kopiranje ovog drugog lanca. Kako se to događa?
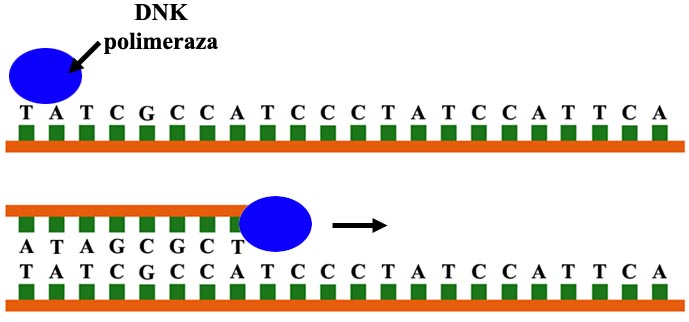
Na lanac DNK se “zakači” enzim (protein) zvani DNK polimeraza. Ovaj enzim onda klizi niz DNK, i dodaje jednu po jednu bazu koja je komplementarna postojećem lancu. Znači, ako naleti na T, on na drugu stranu zakači A. Ako naleti na C, zakači G. Itd.
Pogledajmo ovo na slici:
Ovo izgleda veoma fino, mehanički i uređeno. Ako pogledate neke od mnogobrojnih animacija na Internetu koje prikazuju ovaj proces, videćete kako enzim ide korak po korak, glatko i fino. Prema enzimu “lete” potrebni sastavni delovi, koje on lepo uklapa u celinu. Često su ovakve animacije postavljene sa klasičnom muzikom u pozadini, doprinoseći ideji da se radi o lepom i uređenom “molekularnom plesu”.
Stvarnost je potpuno drugačija. Okolina DNK je ispunjena rastvorenim šećerima, hiljadama vrsta proteina, RNK molekula, energetskim molekulima kao što je ATP, sastavnim delovima RNK (koji se od sastavnih delova DNK razlikuju samo po jednom jedinom atomu kiseonika!), i mnogim drugim stvarima. Ova haotična smesa se haotično kreće: molekuli udaraju jedni o druge, odskaču, naleću, provače se između većih struktura…
Zamislimo da je naša polimeraza u položaju kakav vidimo na donjem delu prethodne slike: iskopirala je jedan deo DNK, i sada se nalazi pored timina (T). Ona sada treba da na novi lanac zakači adenin (A), koji je komplementarna baza timinu. Kako će ona da nađe pravi sastavni deo u svom okolnom haosu?
Odgovor je da uopšte neće tražiti – ona će računati na haos da donese ono što je potrebno! Ona će prosto da stoji i čeka. Na nju će da naklete hiljade različitih molekula različitih vrsta, naelektrisanja, i oblika. Povremeno će na nju da nalete i sastavni delovi DNK, pa i željeni adenin…ali će naleteti pod pogrešnim uglom, ili na pogrešan deo molekula, i prosto će se odbiti i odleteti nazad u haos.
Ali pre ili kasnije, neki molekul koji liči na sastavni deo DNK (po obliku, veličini i naelektrisanju) će naleteti na DNK polimerazu pod pravim uglom, i na pravo mesto. DNK polimeraza reaguje na ovo tako što uhvati taj molekul, i gurne ga fizički prema DNK molekulu koga pokušava da kopira. Ako je u pitanju pogrešan nukleotid – recimo, ako je uhvaćen guanin umesto adenina – on se neće uklopiti sa suprotnom stranom, i biće izbačen iz polimeraze. Ona onda nastavlja da čeka.
Tek kada željena grupa, adenin, naleti pod pravim uglom i sa pravim ubrzanjem, DNK polimeraza će moći da gurne ovaj sastojak na mesto, formira novu hemijsku vezu, i pređe na sledeće “slovo” DNK.
Pogledajmo ovaj proces pažljivo: imamo protein koji visi na DNK. Na njega će naleteti više milijardi različitih molekula, pre nego što naleti pravi molekul pod pravim uglom, i pre nego što ona može da napravi samo jedan jedini korak niz DNK molekul! Na sreću, molekularni pokreti su veoma, veoma brzi; čak i sa ovim ograničenjem, DNK polimeraza može da iskopira preko hiljadu parova u minutu.
Ali ovo nije kraj haosa. I pored sve pažnje, u okviru svakih par hiljada baznih parova, DNK polimeraza će povremeno da udene pogrešno “slovo” – recimo, G nasuprot T. Ovo bi dovelo do nivoa grešaka koji je dopustiv kod prostih organizama, ali koji je potpuno nedopustiv kod kompleksnih, višećelijskih bića kao što su ljudi.
Zbog ovoga, postoji sistem za korekciju grešaka. Pogrešno slovo nije u stanju da stvori pravilne vodonične veze, zbog čega ono izaziva “izbočinu” u spirali DNK. “Zadnji kraj” DNK polimeraze, koji se vuče po DNK iza dela molekula koji kači nova slova, će da uoči tu “izbočinu”, i odseći će pogrešno slovo…nakon čega će da povuče DNK polimerazu nazad, da bi ona udenula pravo slovo na to mesto. Ovo drastično smanjuje broj grešaka, tako da se na kraju u kopiranju događa samo jedna greška na svakih nekoliko desetina hiljada iskopiranih baznih parova.
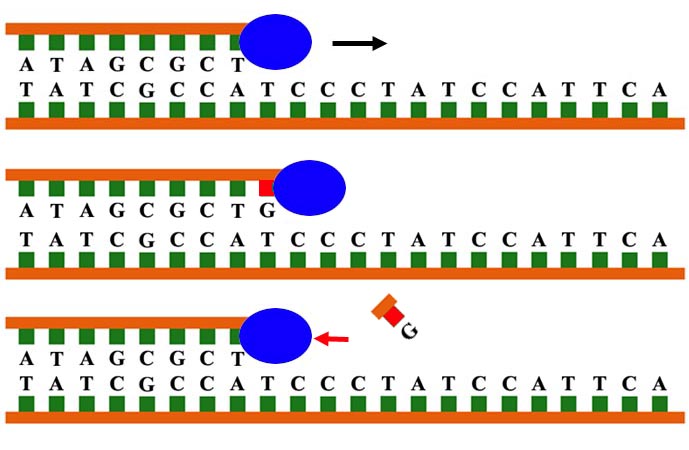
Ono što sada treba imati u vidu je da se sve goreopisano događa kroz ista osnovna pravila fizike i hemije koja smo opisali iznad. Kretanje molekula u okviru mešavine unutar ćelije je slučajno – ali u proseku proizvodi dovoljno pravilnih “udaraca” u DNK polimerazu da bi ona mogla da funkcioniše. Kada sastojak udari na pravi način, pokret kojim polimeraza “gura” taj deo prema potrebnom mestu je potpuno mehanička hemijska promena, zasnovana na činjenici da sastojak “zaklanja” jedan deo molekula od okolne vode.
Isto važi i za ispravku grešaka. Ne postoji neki “vozač” koji sedi na DNK polimerazi i koji je onda vozi unazad kada primeti grešku. Deo molekula DNK polimeraze jednostavno uvek seče vezu kada se veza nađe u određenom položaju – koji je mnogo češći u slučaju greške nego u slučaju pravilno postavljenog dela.
Ovo važi za sve molekule u okviru našeg tela. Pomenuli smo da se pokreti mišića zasnivaju na trilionima molekula miozina koji “hodaju” niz molekule aktina. Ovo je takođe haotičan proces: prvo molekul ATP mora da naleti na miozin pod pravim uglom, koji proizvede hemijsku reakciju. Hemijska reakcija izazove pokret miozina unapred, koji onda u većini slučajeva dovodi do pomeranja molekula. U nekim slučajevima, međutim, on ne uspeva, i molekul ostaje da stoji, ili čak pravi korak unazad. I tako, po principu “tri koraka unapred, jedan korak unazad”, miozin u proseku proizvodi potreban pokret.
Funkcionisanje svakog dela našeg tela se zasniva na slučaju (slučajno pravi molekul mora da pogodi pravu metu pod pravim uglom), proseku (koja funkcija je verovatnija, željena ili neželjena), i termodinamičkom haosu.
Sada, konačno, možemo da se posvetimo temi zbog koje je ovaj tekst uopšte i napisan.
4. Gde se nalazi kompleksnost života?
Čak i najveći kreacionisti priznaju da se i danas u svetu može uživo videti nastanak novih enzima, molekularnih kanala, i sličnih proteina. Kroz promene u genima izazvane slučajnim mutacijama, i kroz izbor koji pravi prirodna selekcija, mi smo videli kako nove molekularne mašine nastaju spontano: male promene u postojećim genima, ili povremeno čak potpuno slučajna sekvenca proizvedena greškom u replikaciji, izaziva nastanak novog gena koji proizvodi novi protein.
Ovi novi proteini funkcionišu kao i svi drugi: u molekularnom haosu ćelije, oni lete kroz prostor dok ne nalete na određenu vrstu mete pod određenim uglom, gde njihov specifičan raspored amino-kiselina proizvede određenu hemijsku reakciju.
Sve ovo se događa bez ikakvog inteligentnog uticaja, zasnovano na osnovnim zakonima hemije i fizike.
Što nas dovodi do pitanja: gde se zaista nalazi kompleksnost živog sveta?
Uzmimo jednu analogiju (veoma nezgrapnu, ali dovoljnu za ilustraciju ovde): zamislimo da umesto proteina i ćelija govorimo o mehaničkim delovima i automobilima. U ovoj analogiji, geni su proste instrukcije kako preseći koje parče metala, gde probušiti rupu, itd. Na kraju procesa, mi ostajemo sa gomilom različitih delova.
Da je naš svet slično organizovan kao molekularni svet, ovi delovi bi se bukvalno sami od sebe sastavili u atomobil. Sve informacije o sastavljanju bi bile sadržane u osnovnim zakonima univerzuma. Takođe, ovaj automobil ne bi morao da ima vozača: sve informacije o saobraćaju, pravilima vožnje, i sve ostalo što je potrebno bi takođe bilo sadržano u osnovnim zakonima. Ovaj automobil ne samo što bi sam sebe sastavio, već bi povrh toga sam sebe vozio!
Razmislimo sada kolika količina informacija je potrebna za jedan “gen” u ovoj analogiji – jedno prosto uputstvo kako napraviti jedan jedini deo automobila. “Uzmi ovakvo parče metala, iseci pod ovakvim uglom, probuši takvu rupu”. To je sve.
A koliko informacija je potrebno da bi se svi ovi delovi sastavili u celinu? Daleko više! Koliko informacija je potrebno za vožnju automobila? Svakako mnogo više nego što je sadržano u bilo kom pojedinačnom “genu!”
Vratimo se sada na život. U okviru organizma stalno nastaju i postoje ogromni kompleksi proteina. Recimo, u ljudskim mitohondrijama, uzmimo samo prvi od četiri transportna centra. Ovaj centar se sastoji od nekoliko desetina proteina, za čije pravilno sklapanje u celinu je potrebna akcija preko sto drugih proteina.
U genima za ove proteine su pohranjene samo informacije o nizu amino-kiselina u svakom od ovih proteina. Ali nigde u genima ne piše kako pravilno saviti bilo koji od njih. Nigde ne piše kako taj protein treba da reaguje kada naleti na neku metu. I pre svega, nigde u genima ne postoji nikakva shema ili informacija o tome kako sastaviti prvi transportni centar!
Ništa od toga nije nigde zapisano u DNK. Nigde ne postoje nikakve informacije o pravilnom sastavljanju transportnog centra, ili o interakcijama potrebnim za to sastavljanje. Sve te informacije “isplivavaju” iz dejstva nekolicine veoma jednostavnih zakona – skoro sve potrebne akcije se odvijaju na osnovu onih pravila koja smo objasnili u prvom delu ovog teksta!
I isto ovo važi za hiljade ovakvih kompleksa, kao i za svaku funkciju u okviru ćelije. Čak i ultrakompleksne funkcije kakve vidimo na sinapsama naših nervnih ćelija, gde ogromni kompleksi proteina vrše desetine hiljada različitih funkcija i gde mreže proteinskih signala kontrolišu nastanak sećanja i procese zaboravljanja…čak i tu važi prethodno. Nijedan deo instrukcija za sklapanje ovakvih kompleksa, niti i jedna jedina komanda o tome kako one treba da funkcionišu nije nigde zapisan u našoj DNK!
Ovo nas dovodi do jednog neizbežnog zaključka: samo jedan mali deo informacija potrebnih za sastavljanje i funkciju bilo kog živog organizma je sadržan u okviru DNK. Najveći deo ovih informacija nastaje u toku samih procesa života, kroz emergentne procese proizvedene kroz interakcije zasnovane na osnovnim, naizgled jednostavnim zakonima hemije i fizike.
Zastupnici ideja kao što je “Inteligentni Dizajn” potpuno propuštaju da primete ovu činjenicu. Njima pojedinačni geni izgledaju “suviše komplikovano” da bi mogli da nastanu kroz prirodne zakone – ne primećujući da daleko veća količina informacija dinamički nastaje upravo tako: iz prirodnih zakona, u okviru najosnovnijih funkcija života.
Kreacionisti koji misle da brane Boga od “ateističke ideje evolucije” prave još veću grešku. Oni pred sobom imaju univerzum u kome mali broj zakona direktno proizvodi samoorganizaciju.
Nakon Velikog Praska, energija se kondenzuje u materiju, vodonik i helijum. Gravitacija izaziva kolaps materije u prve zvezde. U unutrašnjosti zvezda nastaju teži elementi, uključujući o one potrebne za život. Zvezde eksplodiraju i šire ove nove elemente kroz nove nebule gasa i prašine. Ovi oblaci kolapsiraju u nove zvezde, sa planetarnim sistemima. Na odgovarajućim planetama, iz njih nastaje život. I ovaj život se samoorganizuje i evoluira, dok na kraju ne proizvede inteligenciju sposobnu da počne da se pita o svom poreku, i počne da radi na razumevanju univerzuma u kome živi.
I sve ovo, svaki korak, se odigrava na osnovu istih zakona! Iste sile i iste konstante proizvode eksplozije zvezda, formiranje planeta, evoluciju života…i funkciju ćelije danas, pred našim očima.
Vernici mogu da u svemu ovome jasno vide uzvišenog Tvorca, koji je stvorio skoro nezamislivo elegantan sistem savršenih i jednostavnih zakona iz kojih proističe sve što postoji. Umesto toga, oni insistiraju na nekakvom Svetom Tehničaru, koji je sklepao univerzum čiju funkciju mora stalno da “šteluje” i dorađuje. U svom pokušaju da odbrane Boga od nauke, kreacionisti ga u stvari umanjuju i unižavaju.
* * *
Ovaj tekst daje samo osnovne ideje o ovoj temi. Ista emergentna kompleksnost koja je ovde opisana, takođe postoji i na drugim nivoima koji nisu očigledni.
Na primer, pojedinačni mrav je veoma glupa životinja, koja mehanički vrši nekolicinu akcija kao reakciju na hemijske (feromonske) signale. Ali ako skupimo veliki broj ovakvih mrava na gomilu, dobijamo mravinjak, u kome se ova jednostavna ponašanja odjednom sklapaju u neverovatno kompleksne stvari. Mravi imaju poljoprivredu (sade, đubre i uzgajaju određene hranjive gljive), stočarstvo (drže stada drugih insekata, koje onda “muzu” za hranu), organizovanu vojsku (sa generalima, komandantima, strategijom i unapred određenim taktikama napada ili povlačenja), robove (zarobljeni radnici drugih vrsta mrava), inženjering (dva mrava mogu da počnu da kopaju tunel sa različitih strana brda, i da se sretnu tačno u sredini), itd.
Isto tako, naš mozak funkcioniše na osnovu relativno jednostavnih impulsa koji prolaze kroz relativno jednostavne pojedinačne nervne ćelije. Ali u interakciji milijardi ovakvih jednostavnih delova, nastaje neverovatna kompleksnost ljudskog uma.
Primera ima svuda. Samoorganizacija i spontano povećanje kompleksnosti su ugrađeni u naš univerzum, i stoje u njegovim temeljima sa istom važnošću koju ima oponirajuća akcija entropije.
